Diabetes Tipo 2: Fisiopatología, Control Glucémico y Tratamiento Actual
Guía completa sobre diabetes tipo 2: fisiopatología del octeto ominoso, criterios diagnósticos, complicaciones micro y macrovasculares, y tratamiento farmacológico escalonado con metformina, iSGLT2, GLP-1 RA e insulina.
La diabetes mellitus tipo 2 (DM2) es una enfermedad metabólica crónica caracterizada por hiperglucemia persistente, resultado de la combinación de resistencia a la insulina en tejidos periféricos y una disfunción progresiva de la célula beta pancreática. Su importancia en México es crítica: según la Encuesta Nacional de Salud y Nutrición (ENSANUT), la prevalencia alcanza aproximadamente el 14% de la población adulta, posicionándola como la primera causa de mortalidad general, de insuficiencia renal crónica terminal y de amputaciones no traumáticas en el país.
Fisiopatología: El Octeto Ominoso de DeFronzo
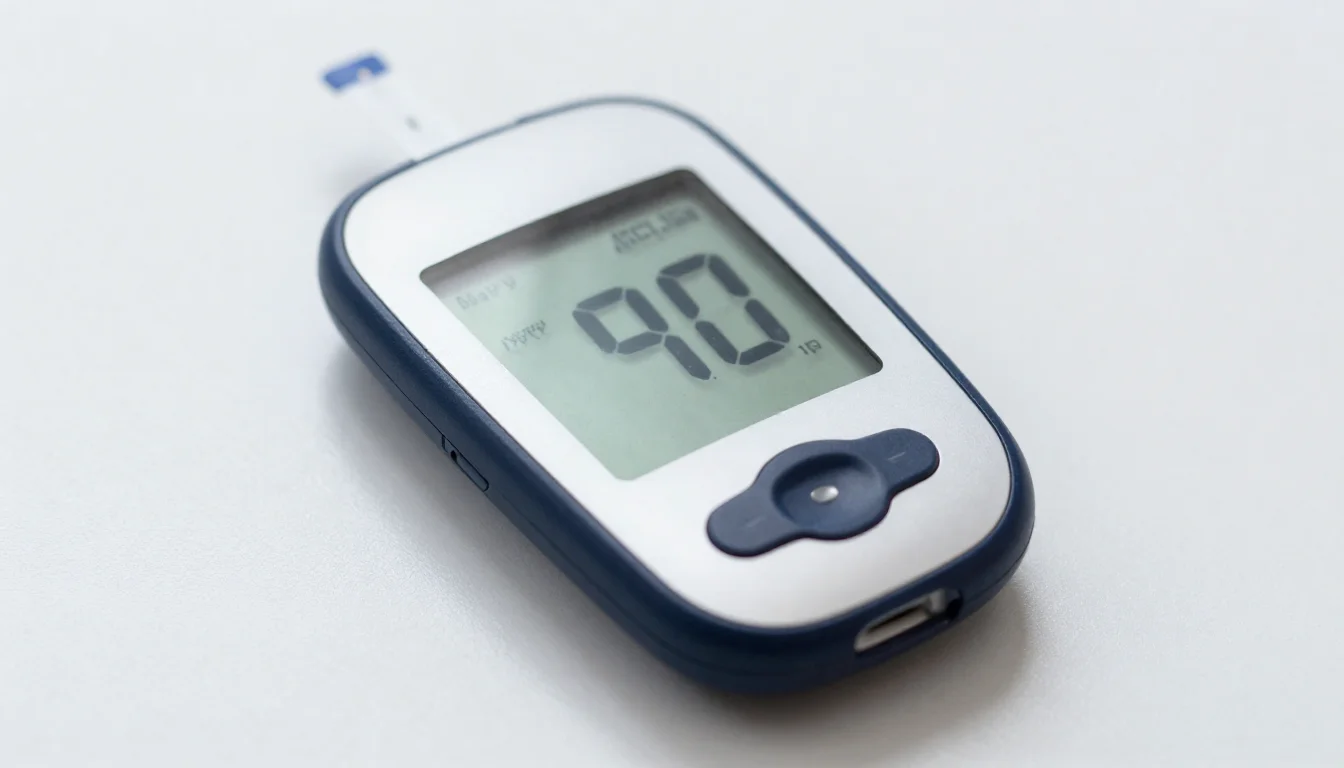
El modelo clásico de resistencia a insulina más falla de célula beta ha sido superado por el concepto del octeto ominoso, propuesto por Ralph DeFronzo, que identifica ocho mecanismos fisiopatológicos simultáneos:
- Resistencia a la insulina en músculo esquelético: Disminución de la captación de glucosa mediada por GLUT-4, con defectos en la señalización postreceptor (IRS-1/PI3K/Akt).
- Aumento de la producción hepática de glucosa: Resistencia hepática a la insulina con gluconeogénesis y glucogenólisis no suprimidas.
- Disfunción progresiva de la célula beta: Pérdida de la primera fase de secreción de insulina, glucotoxicidad y lipotoxicidad que conducen a apoptosis.
- Aumento de la lipólisis en el adipocito: Incremento de ácidos grasos libres circulantes que exacerban la resistencia hepática y muscular.
- Efecto incretina deficiente: Disminución de la secreción de GLP-1 (péptido similar al glucagón tipo 1) y resistencia a GIP, con pérdida del efecto potenciador de la secreción de insulina postprandial.
- Hiperglucagonemia: Secreción inapropiadamente elevada de glucagón por la célula alfa, que aumenta la producción hepática de glucosa.
- Aumento de la reabsorción renal de glucosa: Sobreexpresión de los cotransportadores SGLT2 en el túbulo proximal, que incrementa el umbral de glucosuria.
- Disfunción de neurotransmisores centrales: Resistencia a la insulina en el sistema nervioso central que altera las señales de saciedad y el gasto energético.
Criterios Diagnósticos

La American Diabetes Association (ADA) establece los siguientes criterios, requiriendo confirmación con una segunda prueba en ausencia de hiperglucemia inequívoca:
- Glucosa plasmática en ayuno ≥ 126 mg/dL (ayuno de al menos 8 horas)
- Curva de tolerancia oral a la glucosa (CTOG) ≥ 200 mg/dL a las 2 horas (carga de 75 g de glucosa anhidra)
- Hemoglobina glucosilada (HbA1c) ≥ 6.5% (método estandarizado NGSP/DCCT)
- Glucosa plasmática casual ≥ 200 mg/dL acompañada de síntomas clásicos (poliuria, polidipsia, pérdida de peso inexplicable)
Prediabetes
Se reconocen estados intermedios que confieren riesgo elevado de progresión:
- Glucosa en ayuno alterada: 100-125 mg/dL
- Intolerancia a la glucosa: CTOG 140-199 mg/dL
- HbA1c: 5.7-6.4%
Complicaciones

Complicaciones Microvasculares
- Retinopatía diabética: Principal causa de ceguera en edad productiva. Desde no proliferativa (microaneurismas, exudados) hasta proliferativa (neovascularización). Se requiere revisión oftalmológica anual.
- Nefropatía diabética: Progresión desde microalbuminuria (relación albúmina/creatinina 30-300 mg/g) hasta proteinuria franca y enfermedad renal terminal. Monitoreo con TFGe y RAC al menos anual.
- neuropatía periférica diabética: La más frecuente es la polineuropatía simétrica distal (patrón en guante y calcetín), pero también neuropatía autonómica (gastroparesia, disfunción eréctil, hipotensión ortostática).
Complicaciones Macrovasculares
- infarto al miocardio agudo al miocardio (IAM): La enfermedad cardiovascular es la principal causa de muerte en DM2.
- Evento vascular cerebral (EVC)
- Enfermedad arterial periférica (EAP): Riesgo de úlceras y amputación del pie diabético.
Metas de Control Glucémico
La ADA recomienda una HbA1c < 7% como meta general, pero debe individualizarse:
- Más estricta (< 6.5%): Pacientes jóvenes, sin comorbilidades, diagnóstico reciente, sin hipoglucemia.
- Menos estricta (< 8%): Ancianos frágiles, múltiples comorbilidades, esperanza de vida limitada, historia de hipoglucemia severa.
Tratamiento Farmacológico Escalonado
Primera línea: Metformina
Inhibe la gluconeogénesis hepática mediante activación de AMPK (proteín cinasa activada por AMP). Reduce HbA1c 1.0-1.5%. Efectos adicionales: no produce hipoglucemia, es neutro o favorece leve pérdida de peso. Contraindicada en TFGe < 30 mL/min. Efectos adversos gastrointestinales frecuentes (diarrea, náusea), minimizados con formulación de liberación prolongada.
Inhibidores de SGLT2 (iSGLT2)
Empagliflozina, dapagliflozina, canagliflozina. Bloquean la reabsorción renal de glucosa en el túbulo proximal, induciendo glucosuria de 60-80 g/día. Beneficios cardiovasculares (reducción de eventos MACE y hospitalización por insuficiencia cardíaca) y renales (enlentecimiento de progresión de nefropatía) demostrados en ensayos EMPA-REG, DECLARE-TIMI 58 y DAPA-CKD. Indicados con prioridad en pacientes con enfermedad cardiovascular aterosclerótica, insuficiencia cardíaca o enfermedad renal crónica.
Agonistas del receptor de GLP-1 (GLP-1 RA)
Semaglutida (subcutánea u oral), liraglutida, dulaglutida. Mimetizan la acción de la incretina GLP-1: estimulan la secreción de insulina dependiente de glucosa, suprimen glucagón, retrasan vaciamiento gástrico y promueven saciedad central. Reducen HbA1c 1.0-1.8% y peso corporal 3-7 kg. Beneficio cardiovascular demostrado (SUSTAIN-6, LEADER, REWIND). Inyección subcutánea semanal (semaglutida, dulaglutida) mejora adherencia.
Otras opciones
- Inhibidores de DPP-4 (sitagliptina, linagliptina): Inhiben la degradación de incretinas endógenas. Reducción modesta de HbA1c (0.5-0.8%), neutros en peso, bajo riesgo de hipoglucemia.
- Pioglitazona: Agonista PPARγ, mejora sensibilidad a insulina en músculo y adipocito. Precaución por retención hídrica, aumento de peso, riesgo de fracturas y posible relación con cáncer vesical.
- Sulfonilureas (glibenclamida, glimepirida): Secretagogos de insulina. Efectivas y económicas, pero con riesgo de hipoglucemia y ganancia de peso. Su uso ha disminuido con la disponibilidad de opciones más seguras.
- Insulina: Indicada cuando no se alcanzan metas con agentes orales/inyectables combinados o HbA1c > 10% al diagnóstico. Esquemas: insulina basal (glargina, degludec) como inicio; esquema basal-bolo para optimización.
Estilo de Vida y Automonitoreo
El manejo no farmacológico es pilar fundamental: plan de alimentación individualizado (preferentemente con orientación de nutriólogo), actividad física regular (150 minutos semanales de ejercicio aeróbico moderado más ejercicio de resistencia 2-3 veces por semana), suspensión de tabaquismo y manejo del estrés. El automonitoreo de glucosa capilar o el monitoreo continuo de glucosa (CGM) son herramientas esenciales para ajustar tratamiento y detectar hipoglucemia.
Encuentra especialistas en endocrinologia cerca de ti
Ver todos los especialistasPadecimientos relacionados
¿Tienes alguno de estos padecimientos? Encuentra especialistas verificados cerca de ti.
También te puede interesar

Hipertiroidismo: Síntomas, Causas y Opciones de Tratamiento en México
El hipertiroidismo causa taquicardia, pérdida de peso y ansiedad. Conoce sus causas, la enfermedad de Graves y cuándo consultar a un endocrinólogo.
Hipotiroidismo: Síntomas, Diagnóstico y Tratamiento con Levotiroxina
Guía completa sobre el hipotiroidismo: conoce los síntomas, cómo se diagnostica con pruebas de TSH y T4, y el tratamiento con levotiroxina para regular la tiroides.
Síndrome Metabólico: Diagnóstico, Riesgos y Estrategias de Manejo
El síndrome metabólico: criterios diagnósticos ATP III/IDF, fisiopatología de la resistencia a la insulina y adiposopatía visceral, riesgos cardiovasculares y estrategias de manejo basadas en evidencia.
Equipo Médico Consultorios24
Contenido médico revisado por profesionales de la salud
Este artículo fue creado por nuestro equipo médico editorial y revisado para garantizar su precisión y confiabilidad.
¿Buscas un especialista en endocrinologia?
Encuentra los mejores médicos verificados cerca de ti
Ver especialistas