Enfermedad de Alzheimer: Síntomas Tempranos, Diagnóstico y Cuidados
Información médica sobre enfermedad de Alzheimer: neuropatología amiloide y tau, síntomas por etapa, diagnóstico con biomarcadores y neuroimagen, tratamiento actual y cuidados del paciente.
Definición y contexto epidemiológico

La enfermedad de Alzheimer (EA) es una enfermedad neurodegenerativa progresiva e irreversible que constituye la causa más frecuente de demencia, responsable del 60-70 % de todos los casos. La demencia se define como un deterioro cognitivo adquirido, de magnitud suficiente para interferir con la independencia funcional del individuo en sus actividades cotidianas.
En México, con una población que envejece aceleradamente —se proyecta que los mayores de 65 años representen el 15 % para 2030—, la prevalencia de demencia se estima en 7-8 % en mayores de 60 años, lo que equivale a más de 1.3 millones de personas. El costo social y económico es enorme: cada paciente requiere en promedio 40-70 horas semanales de cuidados, predominantemente proporcionados por familiares.
Neuropatología

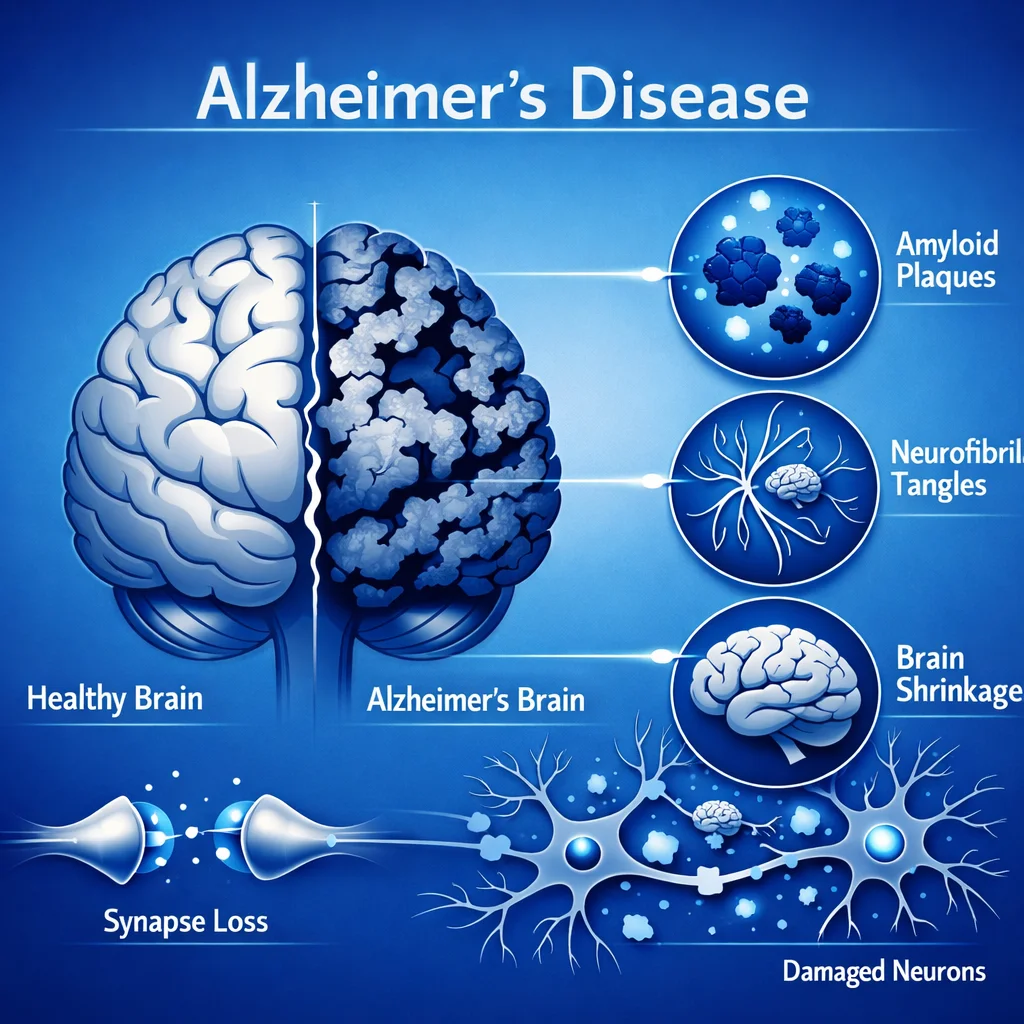
La EA se caracteriza por dos hallazgos histopatológicos cardinales:
Placas amiloides
El péptido beta-amiloide (Aβ), particularmente la isoforma de 42 aminoácidos (Aβ42), se genera por la escisión secuencial de la proteína precursora de amiloide (APP) por las enzimas β-secretasa (BACE1) y γ-secretasa. En condiciones normales, el Aβ se produce y se elimina eficientemente. En la EA, un desequilibrio entre producción y aclaramiento conduce a la acumulación de oligómeros solubles de Aβ —las especies más neurotóxicas— y posteriormente a la formación de placas amiloides extracelulares insolubles.
Los oligómeros de Aβ alteran la función sináptica, inducen estrés oxidativo, activan la microglía y los astrocitos, y promueven una cascada inflamatoria crónica.
Ovillos neurofibrilares
La proteína tau, que normalmente estabiliza los microtúbulos axonales facilitando el transporte intracelular, sufre hiperfosforilación patológica. La tau hiperfosforilada se disocia de los microtúbulos y se agrega en filamentos helicoidales pareados que forman ovillos neurofibrilares intraneuronales. Esto desestabiliza el citoesqueleto, interrumpe el transporte axonal y contribuye a la muerte neuronal.
Pérdida sináptica y neuronal
La pérdida de sinapsis —que correlaciona más estrechamente con el deterioro cognitivo que la carga de placas— es prominente en el hipocampo, la corteza entorrinal, el núcleo basal de Meynert (principal fuente de acetilcolina cortical) y las áreas de asociación neocorticales. La atrofia cerebral progresiva es evidente macroscópicamente.
Factores de riesgo

No modificables
- Edad: el factor más importante. La prevalencia se duplica cada 5 años después de los 65.
- Genotipo APOE ε4: el alelo ε4 de la apolipoproteína E es el factor de riesgo genético más fuerte para EA esporádica. Un alelo ε4 aumenta el riesgo 3-4 veces; dos alelos, 8-12 veces. APOE ε4 reduce la eficiencia del aclaramiento de Aβ.
- Historia familiar: riesgo aumentado con familiares de primer grado afectados.
- Sexo femenino: mayor prevalencia, parcialmente explicada por la mayor longevidad.
Modificables (modelo de la Lancet Commission 2020)
Se estima que hasta el 40 % de los casos de demencia son atribuibles a factores modificables:
- Menor educación formal (baja reserva cognitiva).
- hipertensión arterial en la edad media.
- diabetes tipo 2 (resistencia a insulina cerebral, glicación de proteínas).
- obesidad en la edad media.
- Sedentarismo (el ejercicio promueve neurotrofinas como BDNF).
- Tabaquismo.
- Depresión (puede ser tanto factor de riesgo como pródromo).
- Aislamiento social.
- Pérdida auditiva no corregida.
- Consumo excesivo de alcohol.
- Contaminación ambiental.
- Traumatismo craneoencefálico (TEC): la encefalopatía traumática crónica comparte patología tau.
Deterioro cognitivo leve (DCL)
El DCL representa una fase prodrómica entre el envejecimiento normal y la demencia. Se define como un deterioro cognitivo objetivo (en uno o más dominios) mayor al esperado para la edad y escolaridad, pero que no compromete significativamente la independencia funcional. El subtipo amnésico (DCL-a) tiene la mayor tasa de conversión a EA: 10-15 % anual.
Síntomas por etapa
Etapa temprana (EA leve)
- Pérdida de memoria episódica reciente: olvida conversaciones recientes, repite preguntas, pierde objetos. La memoria remota se conserva relativamente.
- Desorientación temporoespacial: confusión con fechas, dificultad para llegar a lugares conocidos.
- Dificultad para encontrar palabras (anomia incipiente).
- Problemas con la planificación y la toma de decisiones (disfunción ejecutiva).
- Cambios sutiles de personalidad: apatía, irritabilidad, retraimiento social.
Etapa moderada (EA moderada)
- Deterioro marcado de la memoria: no reconoce familiares lejanos, olvida datos autobiográficos importantes.
- Afasia: dificultad progresiva para la expresión y comprensión del lenguaje.
- Apraxia: incapacidad para realizar actos motores aprendidos (vestirse, usar cubiertos) pese a función motora intacta.
- Agnosia: dificultad para reconocer objetos, rostros o sonidos familiares.
- Síntomas neuropsiquiátricos: agitación, agresividad, delirios (paranoia, robo), alucinaciones (predominantemente visuales), vagabundeo, inversión del ciclo sueño-vigilia (sundowning).
- Requiere supervisión para actividades básicas.
Etapa avanzada (EA severa)
- Pérdida casi total de la memoria y el lenguaje (mutismo).
- Dependencia completa para todas las actividades de la vida diaria.
- Dificultad para la deglución (disfagia), riesgo de neumonía por aspiración.
- Incontinencia urinaria y fecal.
- Rigidez, posturas flexoras, inmovilidad.
- Susceptibilidad a infecciones, úlceras por presión, trombosis venosa.
Diagnóstico
Evaluación neuropsicológica
- MMSE (Mini-Mental State Examination): puntuación máxima 30; ≤23 sugiere demencia (ajustar por escolaridad).
- MoCA (Montreal Cognitive Assessment): más sensible que el MMSE para DCL y demencia temprana; evalúa función ejecutiva, visuoespacial, memoria, lenguaje, atención.
- Baterías extensas: CERAD, ADAS-Cog, evaluación de dominios específicos.
Neuroimagen estructural
- RMN cerebral volumétrica: atrofia del hipocampo y la corteza entorrinal (escala de Scheltens para atrofia temporal medial), atrofia cortical posterior, ensanchamiento ventricular. Descarta causas tratables (hidrocefalia normotensiva, hematoma subdural crónico, tumores).
Biomarcadores
El marco ATN (Amiloide-Tau-Neurodegeneración) permite la clasificación biológica:
- A (Amiloide): PET con trazadores amiloides (florbetapir, florbetaben, flutemetamol); Aβ42 disminuido en LCR; cociente Aβ42/40 reducido en sangre.
- T (Tau): PET tau (flortaucipir); p-tau181 y p-tau217 elevados en LCR o plasma.
- N (Neurodegeneración): t-tau elevado en LCR; FDG-PET con hipometabolismo temporoparietal; NfL (neurofilamento de cadena ligera) elevado en sangre.
Los biomarcadores sanguíneos (p-tau217, cociente Aβ42/40 plasmático) están emergiendo como herramientas de tamizaje accesibles y precisas.
Tratamiento
Sintomático
- Inhibidores de colinesterasa: compensan el déficit colinérgico cortical por pérdida neuronal en el núcleo basal de Meynert.
- Donepezilo (5-10 mg/día): el más prescrito, una dosis diaria.
- Rivastigmina (parche transdérmico 4.6-13.3 mg/24 h): inhibe acetilcolinesterasa y butirilcolinesterasa. Parche transdérmico reduce efectos GI.
- Galantamina (8-24 mg/día): inhibición de AChE + modulación alostérica de receptores nicotínicos.
- Indicados en EA leve a moderada. Efectos adversos: náusea, diarrea, arritmias cardíacas.
- Memantina (10-20 mg/día): antagonista no competitivo del receptor NMDA de glutamato. Reduce la excitotoxicidad glutamatérgica. Indicada en EA moderada a severa; puede combinarse con inhibidores de colinesterasa.
Terapias anti-amiloide
- Lecanemab (Leqembi): anticuerpo monoclonal humanizado dirigido contra protofibrillas solubles de Aβ. El estudio CLARITY AD demostró una reducción del 27 % en el declive cognitivo a 18 meses versus placebo en EA temprana. Requiere infusiones IV cada 2 semanas y monitoreo con RMN para ARIA (edema y microhemorragias relacionadas con amiloide).
- Aducanumab (Aduhelm): aprobado por la FDA en 2021 bajo aprobación acelerada; resultados controvertidos y adopción clínica limitada.
- Donanemab: anticuerpo contra la forma piroglumatamada de Aβ; resultados positivos en fase III (TRAILBLAZER-ALZ 2), con posibilidad de discontinuar tras aclaramiento amiloide suficiente.
Estas terapias representan un cambio de paradigma al abordar la patología subyacente, aunque su beneficio clínico es modesto y deben aplicarse en etapas tempranas.
Cuidados del cuidador y estimulación cognitiva
El cuidador primario (frecuentemente un familiar femenino) tiene alto riesgo de depresión, ansiedad y agotamiento. Se recomienda:
- Grupos de apoyo y psicoeducación.
- Respiro del cuidador (centros de día, cuidadores temporales).
- Terapia de estimulación cognitiva: actividades estructuradas que ejercitan la memoria, el lenguaje y las funciones ejecutivas; han demostrado beneficio en EA leve-moderada.
- Modificación ambiental: rutinas consistentes, señalización visual, eliminación de riesgos.
Encuentra especialistas en neurologia cerca de ti
Ver todos los especialistasPadecimientos relacionados
¿Tienes alguno de estos padecimientos? Encuentra especialistas verificados cerca de ti.
También te puede interesar

Derrame Cerebral (ACV): Síntomas de Alerta y Qué Hacer en una Emergencia
Aprende a reconocer los síntomas de un derrame cerebral (ACV), cómo actuar en una emergencia y qué hacer para salvar vidas. Información médica esencial.

Migraña: Síntomas, Tratamiento y Cuándo Consultar al Neurólogo
Guía completa sobre migraña: síntomas, tipos, tratamiento abortivo y preventivo. Descubre cuándo consultar a un neurólogo y cómo controlar las migrañas efectivamente.

Vértigo: Causas, Diagnóstico Diferencial y Tratamiento Efectivo
Guía neurológica sobre vértigo: diferencia periférico vs central, VPPB y maniobra de Epley, neuritis vestibular, enfermedad de Ménière, signos de alarma y rehabilitación vestibular.
Equipo Médico Consultorios24
Contenido médico revisado por profesionales de la salud
Este artículo fue creado por nuestro equipo médico editorial y revisado para garantizar su precisión y confiabilidad.
¿Buscas un especialista en neurologia?
Encuentra los mejores médicos verificados cerca de ti
Ver especialistas