Glaucoma: El Ladrón Silencioso de la Visión - Detección y Tratamiento
Información médica completa sobre glaucoma: tipos, fisiopatología del daño al nervio óptico, diagnóstico con OCT y campimetría, y opciones de tratamiento médico, láser y quirúrgico.
¿Qué es el glaucoma?
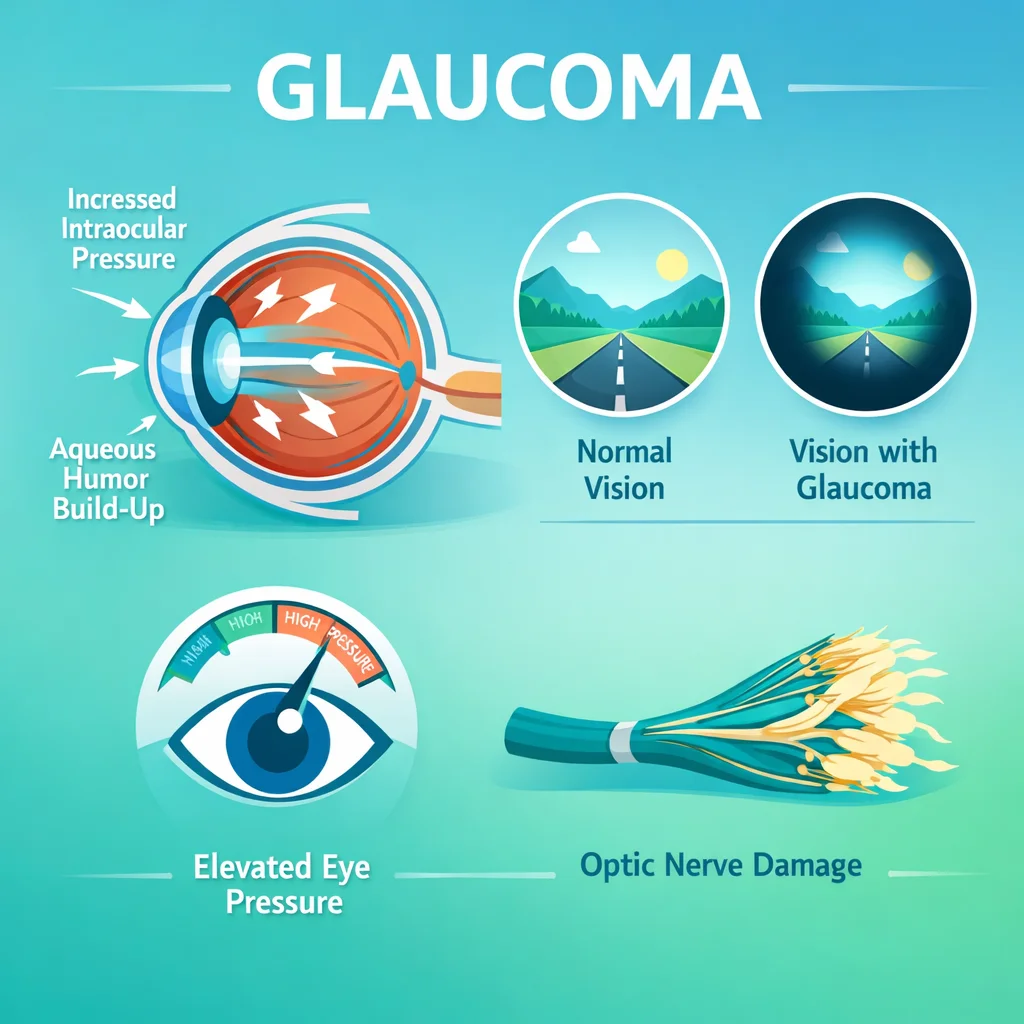
El glaucoma engloba un grupo de neuropatías ópticas progresivas caracterizadas por la pérdida irreversible de células ganglionares de la retina y el adelgazamiento de la capa de fibras nerviosas retinianas (CFNR), con la consecuente excavación del disco óptico y deterioro del campo visual. Constituye la primera causa de ceguera irreversible a nivel mundial, con una prevalencia estimada de 3.5 % en mayores de 40 años.
Lo que hace particularmente peligroso al glaucoma es su naturaleza insidiosa: la pérdida de campo visual comienza en la periferia, donde el paciente no la percibe, y cuando se manifiestan los síntomas centrales el daño ya es extenso e irrecuperable.
Dinámica del humor acuoso
El humor acuoso es un líquido transparente producido por el epitelio no pigmentado del cuerpo ciliar a un ritmo de aproximadamente 2.5 µL/min. Su trayecto sigue este recorrido:
- Se secreta en la cámara posterior.
- Fluye a través de la pupila hacia la cámara anterior.
- Se drena por dos vías:
- Vía trabecular (convencional): atraviesa el trabéculo, el canal de Schlemm y las venas epiesclerales. Responsable del 80-90 % del drenaje.
- Vía uveoescleral (no convencional): difusión a través del músculo ciliar hacia el espacio supracoroideo. Representa el 10-20 % restante.
La presión intraocular (PIO) normal oscila entre 10 y 21 mmHg (media 15.5 mmHg). El desequilibrio entre producción y drenaje del acuoso eleva la PIO, principal factor de riesgo modificable del glaucoma.
Tipos de glaucoma
Glaucoma primario de ángulo abierto (GPAA)
Es la forma más prevalente (70-80 % de todos los glaucomas). El ángulo iridocorneal está abierto, pero existe una resistencia aumentada al flujo en el trabéculo, posiblemente por acumulación de material extracelular, colapso del canal de Schlemm o disfunción de las células trabeculares. La PIO puede estar elevada (>21 mmHg) o normal (glaucoma de tensión normal), donde factores vasculares y de susceptibilidad del nervio óptico desempeñan un papel predominante.
Glaucoma primario de ángulo cerrado
El iris periférico ocluye mecánicamente el trabéculo, impidiendo el drenaje del acuoso. Factores predisponentes: cámara anterior poco profunda, cristalino grueso (hipermetropía), plateau iris. El cierre agudo se presenta como una emergencia oftalmológica: dolor ocular intenso, cefalea, náusea, visión de halos, ojo rojo y PIO >40 mmHg. Requiere tratamiento inmediato con agentes hipotensores e iridotomía láser.
Glaucomas secundarios
Asociados a causas identificables: pseudoexfoliativo (depósitos de material fibrilar en cápsula anterior y trabéculo), pigmentario (liberación de pigmento del iris), neovascular (diabetes, oclusión venosa retiniana), uveítico, cortisónico, traumático, facolítico.
Glaucoma congénito
Anomalía del desarrollo del ángulo camerular. Se presenta en los primeros meses de vida con epífora, fotofobia, buftalmos (aumento del diámetro corneal) y edema corneal. Tratamiento quirúrgico: goniotomía o trabeculotomía.
Factores de riesgo
- PIO elevada: el factor de riesgo modificable más importante.
- Edad >40 años: la prevalencia se duplica cada década después de los 40.
- Raza: mayor prevalencia y severidad en afrodescendientes y latinos.
- Antecedentes familiares: riesgo 4-9 veces mayor en familiares de primer grado.
- Miopía alta: elongación axial asociada a mayor susceptibilidad laminar.
- Espesor corneal central delgado (<520 µm): subestima la PIO real y se asocia de forma independiente con mayor riesgo.
- Diabetes mellitus, hipotensión nocturna, apnea del sueño.
Fisiopatología del daño glaucomatoso
La presión intraocular elevada deforma mecánicamente la lámina cribosa —estructura colágena porosa por donde las fibras del nervio óptico atraviesan la esclera—, comprimiendo los axones y alterando el transporte axoplásmico anterógrado y retrógrado. Esto desencadena:
- Isquemia local por compresión de capilares en la cabeza del nervio óptico.
- Liberación de glutamato excitotóxico.
- Activación de astrocitos y microglía con producción de citocinas proinflamatorias.
- Apoptosis de células ganglionares retinianas.
El resultado morfológico es la excavación progresiva del disco óptico: aumento de la relación copa/disco (C/D), adelgazamiento del anillo neurorretiniano, muescas, hemorragias en astilla y atrofia peripapilar.
Diagnóstico
Tonometría
Medición de la PIO. El estándar es la tonometría de aplanamiento de Goldmann. Alternativas: tonómetro de rebote (iCare), tonómetro de contorno dinámico (Pascal).
Gonioscopia
Evaluación directa del ángulo iridocorneal con lente de contacto prismática. Clasifica el ángulo según Shaffer o Spaeth e identifica sinequias, neovascularización o depósitos pigmentarios.
Campimetría (perimetría automatizada)
Evalúa la función del campo visual. El Humphrey 24-2 SITA-Standard es el protocolo más utilizado. Detecta escotomas arciformes, escalón nasal, depresión generalizada. Requiere al menos dos campos visuales confiables para confirmar daño.
Tomografía de coherencia óptica (OCT)
Cuantifica objetivamente el espesor de la CFNR peripapilar y el complejo de células ganglionares macular. Detecta pérdida estructural antes de que sea evidente en la campimetría (daño preclínico). Las bases de datos normativas permiten comparar con población sana por edad.
Paquimetría
Medición del espesor corneal central. Córneas delgadas subestiman la PIO con tonometría de Goldmann y son un factor de riesgo independiente.
Tratamiento
Tratamiento médico (gotas hipotensoras)
El objetivo es reducir la PIO a un nivel que detenga la progresión (PIO objetivo individualizado, generalmente un 20-30 % de reducción).
- Análogos de prostaglandinas (latanoprost, travoprost, bimatoprost, latanoprosteno bunod): primera línea. Aumentan el flujo uveoescleral. Una gota nocturna, reducción de 25-35 %.
- Betabloqueadores (timolol, betaxolol): reducen la producción de acuoso. Contraindicados en asma, EPOC, arritmias cardíacas.
- Alfa-agonistas (brimonidina): reducen producción y aumentan flujo uveoescleral. Efecto neuroprotector potencial.
- Inhibidores de anhidrasa carbónica (dorzolamida, brinzolamida; acetazolamida oral): disminuyen la producción de acuoso.
- Inhibidores de Rho-kinasa (netarsudil): aumentan el drenaje trabecular, único mecanismo que aborda directamente la fisiopatología del GPAA.
- Combinaciones fijas: PG + timolol, brimonidina + timolol, entre otras; mejoran la adherencia al reducir el número de gotas.
Tratamiento con láser
- Trabeculoplastia selectiva (SLT): láser Nd:YAG de pulso corto aplicado al pigmento del trabéculo. Estimula la remodelación celular sin daño térmico. Eficacia comparable a las gotas como primera línea (estudio LiGHT). Repetible.
- Iridotomía periférica con Nd:YAG: tratamiento del cierre angular. Crea una comunicación entre cámara anterior y posterior que elimina el bloqueo pupilar.
- Ciclofotocoagulación: destrucción parcial del cuerpo ciliar para reducir producción de acuoso. Reservada para glaucomas refractarios.
Tratamiento quirúrgico
- Trabeculectomía: creación de una fístula protegida desde la cámara anterior al espacio subconjuntival (ampolla filtrante). Eficaz pero con riesgos de hipotonía, endoftalmitis de ampolla y fibrosis. Se utiliza antimetabolito (mitomicina C) para inhibir la cicatrización.
- Dispositivos de drenaje (válvula de Ahmed, implante de Baerveldt): tubo que drena el acuoso a un reservorio subconjuntival. Indicados en glaucomas refractarios o con alto riesgo de fibrosis.
- MIGS (Micro-Invasive Glaucoma Surgery): iStent, Hydrus, goniotomía con Kahook, Xen Gel Stent. Procedimientos ab interno con menor perfil de complicaciones, reducción modesta de PIO, frecuentemente combinados con cirugía de catarata.
Importancia del tamizaje
Se recomienda una evaluación oftalmológica completa que incluya medición de PIO, evaluación del disco óptico y, si existen factores de riesgo, campimetría y OCT, a partir de los 40 años. La detección temprana y el tratamiento oportuno pueden preservar la visión de por vida.
Encuentra especialistas en oftalmologia cerca de ti
Ver todos los especialistasPadecimientos relacionados
¿Tienes alguno de estos padecimientos? Encuentra especialistas verificados cerca de ti.
También te puede interesar

Retinopatia Diabetica: Sintomas, Etapas y Cuando Consultar al Oftalmologo
La retinopatia diabetica afecta al 31% de diabeticos en Mexico. Conoce sus sintomas, etapas y cuando consultar al oftalmologo para proteger tu vision.
Glaucoma: Síntomas Silenciosos y la Importancia de la Detección Temprana
El glaucoma es llamado "el ladrón silencioso de la vista". Conoce sus síntomas, factores de riesgo y por qué la detección temprana puede salvar tu visión.
Conjuntivitis: Síntomas, Causas y Tratamiento del Ojo Rojo
La conjuntivitis es una infección ocular muy común. Aprende a identificar sus síntomas, tipos y el tratamiento adecuado para cada caso.
Equipo Médico Consultorios24
Contenido médico revisado por profesionales de la salud
Este artículo fue creado por nuestro equipo médico editorial y revisado para garantizar su precisión y confiabilidad.
¿Buscas un especialista en oftalmologia?
Encuentra los mejores médicos verificados cerca de ti
Ver especialistas